Allergie aux corticoïdes
1. Rappels pharmacologiques
1.1. Corticoïdes naturels
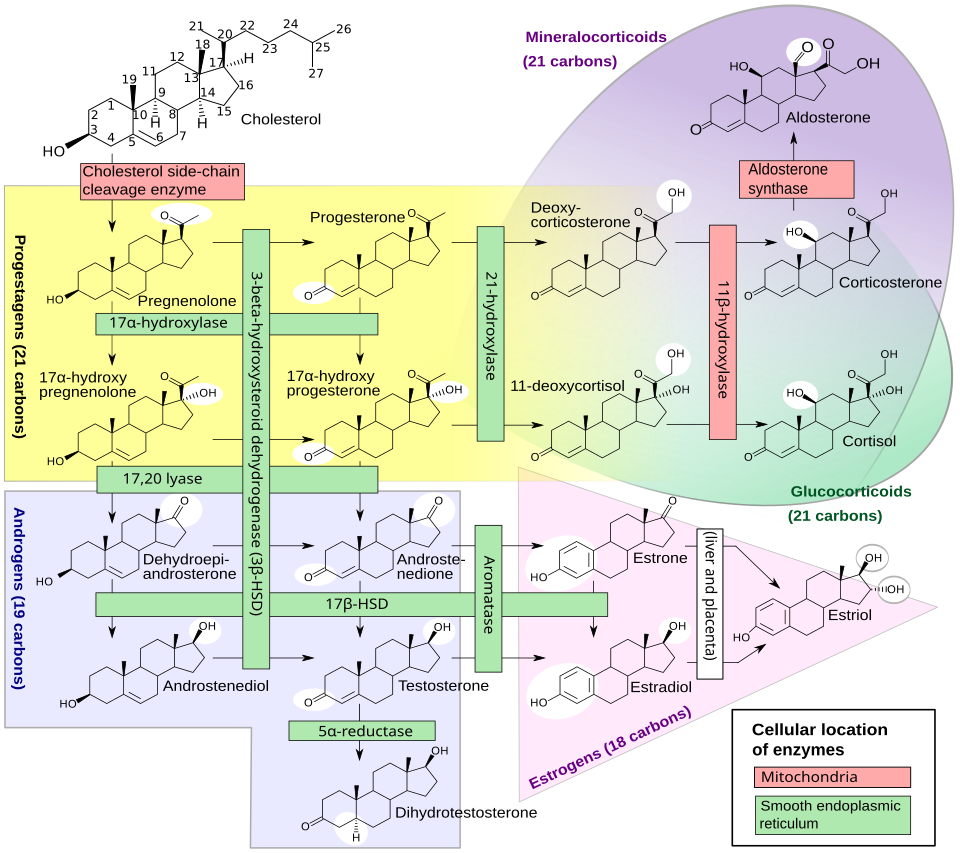
Les corticostéroïdes (corticoïdes) sont des hormones dérivées du cholestérol, produites par les glandes surrénales. Les deux grandes familles physiologiques sont les glucocorticoïdes, dont le chef de file est le cortisol (= hydrocortisone), dotés d’un puissant effet anti-inflammatoire, et les minéralocorticoïdes, représentés par l’aldostérone, qui régulent l’équilibre hydro-sodé rénal. Le présent travail se concentre sur les médicaments reproduisant l’effet glucocorticoïde.
1.2. Importance des corticoïdes de synthèse
Utilisés depuis la fin des années 1940, les corticoïdes constituent l’un des piliers de la thérapeutique anti-inflammatoire et immunosuppressive (Hodgens & Sharman, 2025). Au Royaume-Uni, ils figurent parmi les 10 classes médicamenteuses les plus coûteuses, couvrant 6,4 % des dépenses publiques en médicaments (Prescription Cost Analysis – England 2020-21, NHSBSA). En moyenne, 3,8 % de la population bénéficie d’une prescription de corticoïdes oraux par an, 0,5 à 0,7 % en consommant de façon chronique (> 90 jours/an), la prednisolone étant la molécule la plus prescrite (Bjornsdottir et al., 2024). Au Danemark, 20 à 25 % de la population reçoit une cure de corticoïdes tous les 5 ans, pour une durée médiane de 6 jours (Wallace et al., 2023).
1.3. Classification chimique
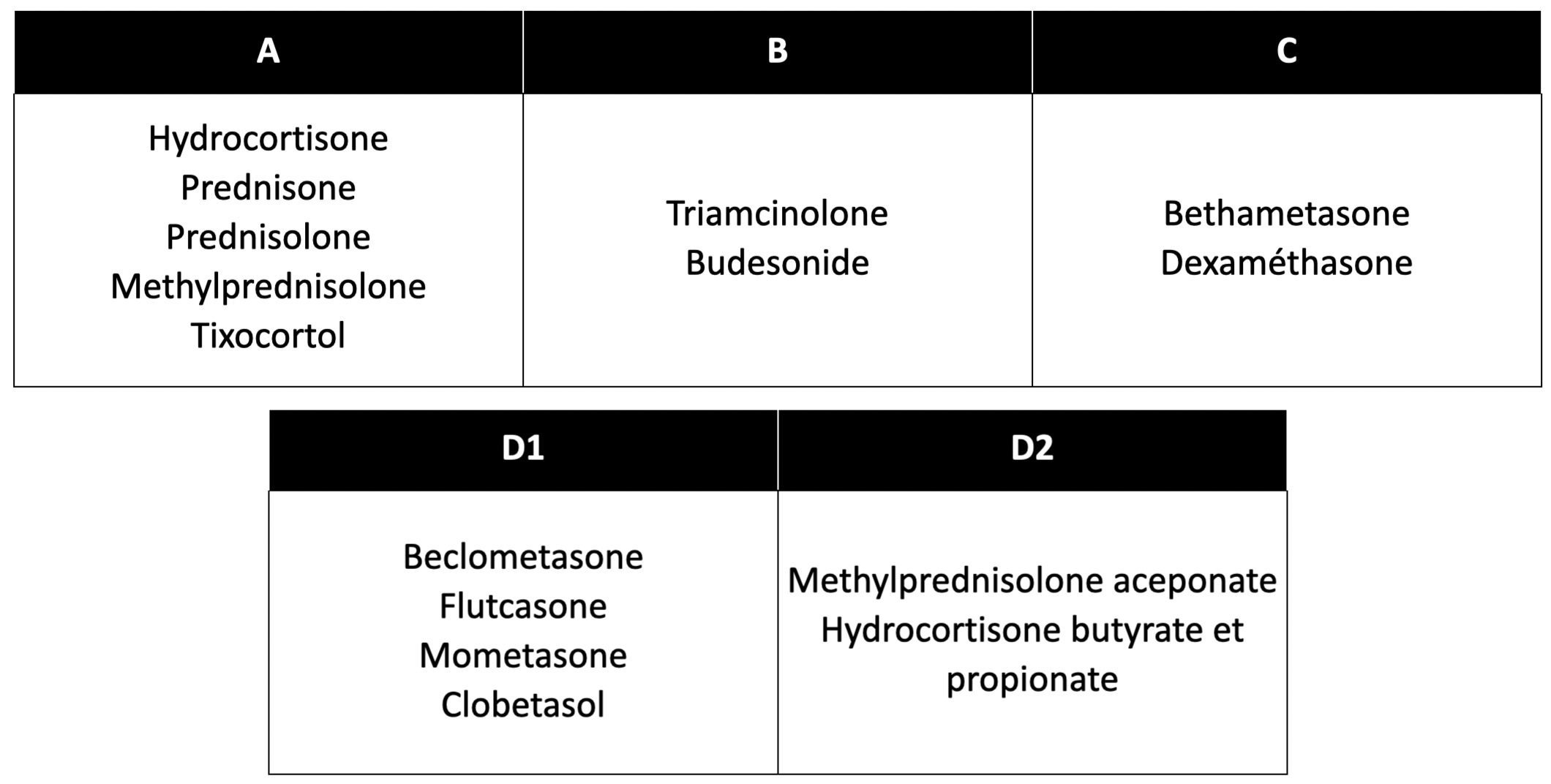
Tous les corticoïdes partagent un squelette cyclopentanoperhydrophénanthrène. Les modifications chimiques de ce noyau (halogénation, méthylation en C16, estérification) modulent la pénétration, la puissance et le profil de sensibilisation allergique. La classification de référence, développée par Coopman et al. en 1989 et révisée par Matura pour le groupe D, distingue quatre groupes (Coopman et al., 1989 ; Matura & Goossens, 2000 ; Mahlab-Guri et al., 2023) :
-
Groupe A (type hydrocortisone) : le plus allergisant en réaction retardée, réactions croisées fréquentes avec le groupe B et D2.
-
Groupe B (type triamcinolone) : deuxième par ordre de fréquence allergique.
-
Groupe C (type bétaméthasone) : très peu de réactions allergiques rapportées.
-
Groupe D1 (esters stables, type bétaméthasone dipropionate) : réactivité modérée.
-
Groupe D2 (esters labiles, type méthylprednisolone acéponate) : réactivité faible.
Cette classification est surtout pertinente pour les réactions retardées (type IV). Elle a été affinée par Baeck et al. en 2011 à l’aide de modèles moléculaires tridimensionnels, proposant trois clusters de réactivité croisée (Baeck, Chemelle, Goossens et al., 2011) :
-
Cluster I : essentiellement groupes A et D2, sans méthylation en C16 ni halogénation, incluant le budésonide.
-
Cluster II : surtout groupe B, molécules halogénées avec structure cis-cétal ou diol en C16/C17.
-
Cluster III : groupes C et D1, molécules halogénées et méthylées en C16 — capacité de sensibilisation la plus faible (Baeck, Chemelle, Rasse et al., 2011).
1.4. Estérification et excipients
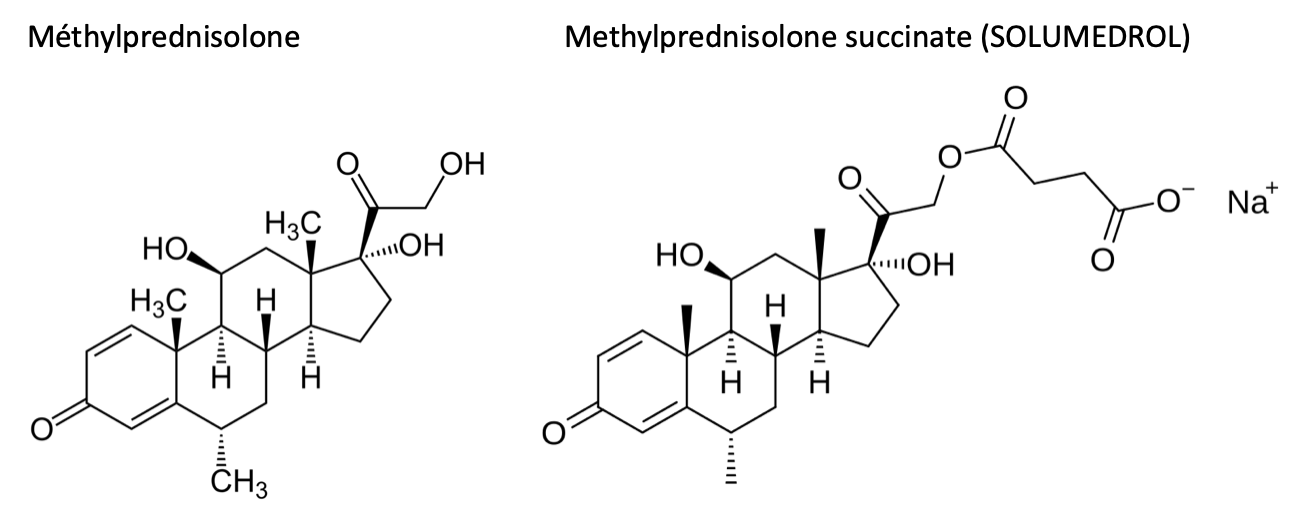
Pour améliorer leur solubilité, certains corticoïdes sont estérifiés avec des groupes hydrophiles (succinate, phosphate). Ces formes estérifiées se comportent comme des entités moléculaires distinctes sur le plan allergique : l’allergie peut porter sur le complexe corticoïde-ester et non sur l’une des deux molécules isolément (Angel-Pereira et al., 2014 ; Walker et al., 2010). L’archétype est la méthylprednisolone succinate (Solumédrol®).
2. Allergie aux corticoïdes : généralités
L’allergie aux corticoïdes constitue un paradoxe apparent : une molécule immunosuppressive qui devient elle-même allergène. Elle repose sur une sensibilisation préalable et se distingue des effets indésirables pharmacologiques (type A) et des réactions d’hypersensibilité non allergique (flush, intolérances, type B). Bien que rare, sa fréquence est cliniquement significative en raison de l’utilisation massive de ces médicaments. On distingue les réactions immédiates (type I, IgE-médiées ou pseudo-allergiques) et les réactions retardées (type IV, à médiation cellulaire T) (Berbegal et al., 2016).
3. Réactions d’hypersensibilité immédiate
3.1. Épidémiologie
La prévalence des réactions immédiates aux corticoïdes systémiques est estimée à 0,1–0,3 % des patients sous corticothérapie (Freymond et al., 2003 ; Klein-Gitelman & Pachman, 1998), mais aucune étude à grande échelle n’a été réalisée (Borja et al., 2001). Seulement 120 réactions ont été colligées dans la littérature entre 2004 et 2014, avec un âge médian de 26 ans, un sex-ratio équilibré et un intervalle d’âge de 2 à 90 ans (Patel & Bahna, 2015).
3.2. Facteurs de risque et voies d’administration
Le terrain atopique et l’exposition répétée constituent les principaux facteurs de risque. La sensibilisation est majoritairement systémique, rarement topique. La voie intraveineuse est la plus fréquemment impliquée (45 %), suivie des voies intra-articulaire (19 %) et orale (15 %) (Patel & Bahna, 2015 ; Baker et al., 2015). Un même patient peut développer une anaphylaxie par plusieurs voies différentes — orale, cutanée, intramusculaire (Erdmann et al., 2005). Il est important de noter que la sensibilisation initiale peut s’effectuer par voie cutanée.
3.3. Molécules impliquées
Le corticoïde le plus fréquemment en cause est la méthylprednisolone (classe A), représentant jusqu’à 50 % des cas dans certaines séries, suivie de la prednisolone (A), la triamcinolone (B) et l’hydrocortisone (A) (Patel & Bahna, 2015). La bétaméthasone et la dexaméthasone (classe C) sont beaucoup mieux tolérées, avec seulement quelques cas isolés décrits (Berbegal et al., 2016).
3.4. Rôle des excipients
Jusqu’à 30–37 % des réactions immédiates attribuées aux corticoïdes sont en réalité des allergies aux excipients, notamment dans les formes retard : carboxyméthylcellulose (CMC), polyéthylène glycol (PEG) et polysorbates (Barbaud, 2014 ; Bruusgaard-Mouritsen et al., 2022 ; Li et al., 2018). Les excipients peuvent varier entre médicament princeps et génériques. Le diagnostic doit donc systématiquement les explorer (Li et al., 2018).
3.5. Réactions croisées en hypersensibilité immédiate
Il n’existe pas de données suffisantes pour prédire les réactions croisées IgE-médiées entre corticoïdes (Barbaud et al., 2024). Cependant, la plupart des patients tolèrent au moins un corticoïde alternatif (Patel & Bahna, 2015), et des patients peuvent tolérer des corticoïdes de la même classe chimique que celui incriminé (Aranda et al., 2010 ; Ben Said et al., 2010). Les formes estérifiées (succinate, phosphate) fonctionnent comme des néo-antigènes : l’allergène est le complexe corticoïde-ester (Angel-Pereira et al., 2014 ; Walker et al., 2010).
3.6. Démarche diagnostique — réactions immédiates
Tests cutanés
-
Prick tests : utiliser la forme pure non diluée (Walker et al., 2010).
-
IDR : dilutions de 1/1 000 à 1/10. La combinaison prick + IDR atteint une sensibilité de 74,1 % ; la spécificité semble élevée mais n’est pas précisément chiffrée (Walker et al., 2010). Certains auteurs déconseillent les IDR en raison du risque d’atrophie cutanée.
-
Tester systématiquement la molécule suspectée, les excipients, et les co-expositions (désinfectant, latex, anesthésiques locaux) (Baker et al., 2015).
-
Les protocoles de concentration recommandés pour chaque molécule sont décrits dans le position paper EAACI/ENDA (Barbaud et al., 2024).
Biologie
-
Les IgE spécifiques n’ont pas démontré d’utilité diagnostique dans ce contexte.
-
Test d‘activation des basophiles (TAB) : prometteur mais non utilisé en routine. Sur 10 cas étudiés entre 2004 et 2014, 7 TAB se sont révélés positifs (Walker et al., 2010 ; Ben Said et al., 2010).
Test de provocation
En raison du manque de données sur la spécificité des tests cutanés, un test de provocation est systématiquement recommandé pour identifier une alternative tolérée (Mahlab-Guri et al., 2023). Il doit être réalisé au moins 1 semaine après les tests cutanés, car les patchs et IDR peuvent induire une positivation retardée (Barbaud et al., 2024). La dose cible peut atteindre 1 mg/kg/jour par voie IV ou IM pour les formes injectables (Padial et al., 2005). La bétaméthasone, la dexaméthasone ou le déflazacort (non commercialisé en France) sont les alternatives de première intention (Ventura et al., 2003).
3.7. Diagnostic différentiel : le flush aux corticoïdes
Vasodilatation transitoire non IgE-médiée se manifestant par un érythème brutal du visage, du cou, du haut du torse et du dos, avec sensation de chaleur. Peut être œdémateuse mais ne gratte pas. Survient 2 à 48 heures après l’injection, dure de quelques minutes à 4 jours. Plus fréquent chez la femme (ratio 3:1) et en cas de rosacée. Les doses élevées sont un facteur favorisant. Pas systématiquement molécule-dépendant. Résolution spontanée. Pas de contre-indication à la poursuite du corticoïde (Kamel et al., 2024 ; Pecquet, 2002 ; Pattrick & Doherty, 1987).
4. Réactions d’hypersensibilité retardée
4.1. Épidémiologie
Les réactions retardées aux corticoïdes sont beaucoup plus fréquentes que les réactions immédiates. La prévalence de la sensibilisation de contact est estimée entre 2,2 et 5 % de la population selon les séries (Dooms-Goossens et al., 1996 ; Bircher et al., 1995), avec 4,6 % de sensibilisation aux États-Unis et 2,6 % en Europe (Jacob & Steele, 2006). Ces variations reflètent en partie des différences de concentration des patch tests et de pratiques de dépistage. En 2005, les corticoïdes ont été nommés « allergène de contact de l’année » par l’European Society of Contact Dermatitis.
4.2. Facteurs de risque
-
Âge avancé (Svendsen et al., 2022).
-
Altération de la barrière cutanée : dermatose chronique, dermatite atopique, insuffisance veineuse.
-
Utilisation prolongée ou répétée de corticoïdes topiques (Mahlab-Guri et al., 2023).
-
Possibilité d’une prédisposition génétique : association HLA évoquée mais non confirmée à grande échelle (Wilkinson et al., 1993 ; Berbegal et al., 2016).
4.3. Présentation clinique
La forme principale est l’eczéma de contact, apparaissant quelques heures à quelques jours après l’application du corticoïde. Les difficultés diagnostiques sont considérables : les signes cliniques peuvent être masqués par l’effet anti-inflammatoire intrinsèque du corticoïde, aboutissant à un tableau de non-réponse thérapeutique ou d’aggravation paradoxale d’une dermatose corticosensible. Une amélioration après arrêt de la corticothérapie est un signe d’alerte majeur (Berbegal et al., 2016). Il est recommandé de rechercher une allergie aux corticoïdes devant toute corticothérapie locale inefficace : 22 % des patients ne répondant pas aux dermocorticoïdes ont un patch test positif (Gönül & Gül, 2005).
Autres formes décrites : pustulose exanthématique aiguë généralisée (PEAG), dermatite exfoliante, érythème multiforme (Stingeni et al., 1996), érythème pigmenté fixe (Mur et al., 2005), et des formes généralisées érythémateuses, maculo-papuleuses, papulo-vésiculeuses, purpuriques ou eczématiformes, voire des érythrodermies (Baeck et al., 2009).
4.4. Formes selon la voie d’administration
Voie cutanée (la plus fréquente)
Le tableau classique est celui d’une dermatose corticosensible qui ne répond pas — voire s’aggrave — sous traitement topique. Des cas d’angiœdème, d’érythème multiforme et de PEAG sont également décrits après application locale (Pirker et al., 2003 ; Stingeni et al., 1996 ; Mur et al., 2005).
Voie inhalée
L’inhalation de corticoïdes (budésonide principalement) peut provoquer un œdème facial et muqueux, un érythème du cou, voire un angiœdème avec dysphagie (Pirker et al., 2003 ; Voltolini & Fumagalli, 2021). La sensibilisation croisée est possible avec d’autres molécules du même groupe. Fait notable, des cas de sensibilisation « par procuration » (by proxy) ont été rapportés chez des personnes vivant au domicile d’un patient sous aérosol de budésonide (Baeck & Goossens, 2009).
Voie nasale et oculaire
L’application de sprays nasaux ou de collyres contenant des corticoïdes peut induire un eczéma périoculaire et/ou facial, une conjonctivite et un larmoiement (Baeck, De Potter & Goossens, 2011). L’hydrocortisone est la molécule la plus souvent en cause dans cette localisation.
Voie systémique : dermatite de contact systémique (SCD)
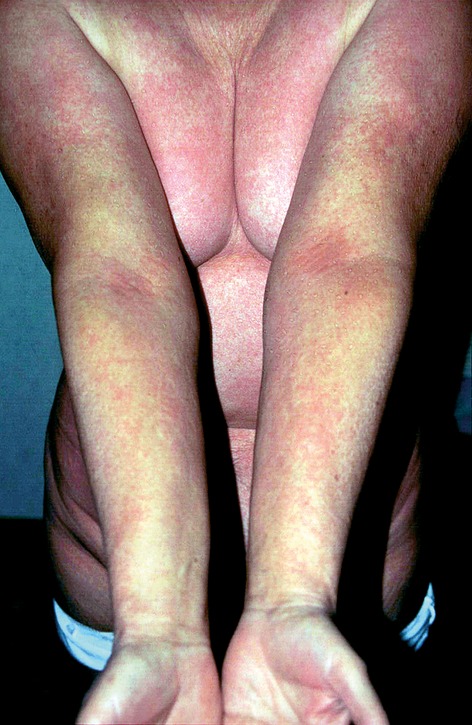
La dermatite de contact systémique (systemic contact dermatitis, SCD) survient lorsqu’un patient préalablement sensibilisé par voie topique reçoit le même corticoïde ou un corticoïde apparenté par voie systémique. Représentant jusqu’à 5 % des cas d’allergie de contact aux corticoïdes, elle se manifeste typiquement par une éruption eczématiforme généralisée, s’accompagnant parfois d’une réactivation sur les zones précédemment atteintes par la réaction locale (Baeck & Goossens, 2012 ; Kulberg et al., 2014). La réaction est limitée à la peau (pas de risque d’anaphylaxie, car la présentation antigénique est assurée par les cellules de Langerhans cutanées). L’éruption régresse spontanément en 15 jours environ après arrêt des corticoïdes.
Les patients atteints de SCD sont souvent polysensibilisés à des molécules de plusieurs classes, correspondant au profil 2 de la classification de Baeck (allergie au squelette stéroïdien). Ils nécessitent une évaluation approfondie de leur profil de tolérance (Baeck & Goossens, 2012).
4.5. Molécules et réactions croisées
Les molécules les plus fréquemment sensibilisantes en réaction retardée sont le budésonide, le tixocortol-21-pivalate et l’hydrocortisone-17-butyrate (chacune sensibilisant plus de 1 % de la population) (Svendsen et al., 2022). Le budésonide arrive en tête en Espagne, le tixocortol aux États-Unis. À eux deux, budésonide et tixocortol détectent 91,3 % des patients sensibilisés aux corticoïdes (Boffa et al., 1995), mais étant tous deux du cluster I, ils peuvent manquer une sensibilisation isolée aux clusters II ou III.
L’ordre de fréquence des familles allergisantes est A > B > D1 ; la famille C donne très peu de réactions (Baeck et al., 2009). Les réactions croisées retardées sont fréquentes entre les groupes A, B et D2. Environ 40 % des patients ayant un patch test positif réagissent à plusieurs corticoïdes, et 6 % réagissent à des corticoïdes de cinq classes différentes (Baeck et al., 2009).
Profils de patients (Baeck, Chemelle, Goossens et al., 2011)
-
Profil 1 — allergie à la chaîne latérale : sensibilisation au cluster I uniquement. La charge moléculaire portée par les substituants est déterminante. Il est possible de réintroduire un corticoïde d’une autre classe après test négatif.
-
Profil 2 — allergie au squelette stéroïdien : sensibilisation aux clusters I + II et/ou III. La structure tridimensionnelle (champ stérique) est déterminante. Ces patients nécessitent une évaluation exhaustive de leur profil de tolérance et, dans les cas les plus sévères (réactivité à toutes les molécules accessibles), l’utilisation des corticoïdes est réservée aux situations d’urgence vitale (Baeck & Goossens, 2012 ; Berbegal et al., 2016).
4.6. Démarche diagnostique — réactions retardées
Patch tests (méthode de référence)
-
Retrait à 48 h, lectures à J2, J4 et J7, selon les recommandations de l’International Contact Dermatitis Research Group (Baeck & Goossens, 2012).
-
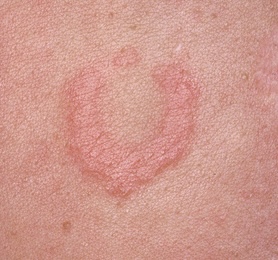
Piège diagnostique — l‘effet bord (edge effect) : anneau d’eczéma périphérique avec centre sain, dû à la concentration plus élevée de corticoïde au centre du patch qui bloque localement la réaction. Plus fréquent aux lectures précoces (Baeck, Marot et al., 2009 ; Berbegal et al., 2016).
-
Piège diagnostique — faux négatif : blanchiment cutané par vasoconstriction pouvant masquer la réaction à 48 h. D’où l’importance des lectures tardives.
-
Les prick tests sont inutiles dans les réactions retardées.
-
Les IDR sont à éviter (risque d’atrophie cutanée) (Isaksson et al., 2000).
Séries de patch tests standardisées
-
Série standard européenne : budésonide, tixocortol-21-pivalate.
-
TRUE test (36 allergènes) : budésonide, tixocortol-21-pivalate, hydrocortisone-17-butyrate.
-
North American Contact Dermatitis Group : budésonide, tixocortol-21-pivalate, hydrocortisone-17-butyrate.
-
Série spécifique corticoïdes (Chemotechnique) : inclut en sus triamcinolone acétonide, dexaméthasone-21-phosphate, clobétasol-17-propionate, bétaméthasone-17-valérate, alclométasone-17,21-dipropionate (tous à 1 % dans la vaseline).
Test de provocation
Un test de provocation orale est recommandé au moins 1 semaine après les patch tests, en utilisant le même produit et la même voie d’administration que ceux impliqués cliniquement (Barbaud et al., 2024). Il est indispensable pour confirmer la pertinence clinique de la sensibilisation et identifier une alternative tolérée.
5. Physiopathologie de l’allergie retardée
L’hypothèse haptène constitue le modèle physiopathologique principal : le corticoïde (ou son produit de dégradation) se lie de manière irréversible aux groupements arginine-guanidine des protéines sériques, formant un néo-antigène capable d’être présenté par les cellules de Langerhans aux lymphocytes T. Les molécules les plus allergisantes sont celles dont les métabolites ont la plus forte capacité de liaison à ces résidus protéiques. Les molécules méthylées en C16 (cluster III) présentent la plus faible capacité de sensibilisation et sont les moins impliquées dans les réactions croisées (Baeck, Chemelle, Rasse et al., 2011).
6. Conduite pratique
6.1. Quand suspecter une allergie aux corticoïdes ?
-
Absence de réponse ou aggravation d’une dermatose corticosensible sous traitement topique.
-
Amélioration paradoxale après arrêt de la corticothérapie.
-
Réaction systémique rapide (urticaire, angiœdème, anaphylaxie) après administration systémique.
-
Éruption généralisée retardée après introduction d’un corticoïde systémique chez un patient utilisant des dermocorticoïdes.
-
Persistance des symptômes malgré un traitement correctement conduit.
6.2. Algorithme diagnostique
-
Réaction immédiate : prick + IDR (molécule, excipients, co-expositions) → TAB si disponible → test de provocation avec alternative sûre (bétaméthasone, dexaméthasone, déflazacort).
-
Réaction retardée : patch tests (série standard + molécules du patient + série spécifique corticoïdes + excipients) avec lectures J2, J4, J7 → test de provocation au moins 1 semaine après.
6.3. Alternatives thérapeutiques
Lorsque le profil de sensibilisation restreint les options corticoïdes disponibles, les alternatives suivantes peuvent être envisagées :
-
Inhibiteurs de la calcineurine topiques (tacrolimus, pimécrolimus).
-
Inhibiteurs de JAK topiques (ruxolitinib).
-
Thérapies ciblées (biothérapies) selon l’indication.
7. Points clés
-
Les réactions retardées (eczéma de contact) sont beaucoup plus fréquentes (2–5 %) que les réactions immédiates (0,1–0,3 %).
-
La classification chimique (A/B/C/D1/D2) et les clusters moléculaires de Baeck guident la compréhension des réactions croisées et le choix des alternatives.
-
En réaction immédiate : penser systématiquement aux excipients (jusqu’à 37 % des cas), notamment CMC et PEG.
-
En réaction retardée : penser à l’effet bord et au faux négatif par blanchiment ; lecture tardive à J7 indispensable.
-
La classe C (bétaméthasone, dexaméthasone) est la mieux tolérée dans les deux types de réactions.
-
Le flush aux corticoïdes est une réaction pseudo-allergique bénigne, ne contre-indiquant pas le traitement.
-
Un test de provocation est toujours recommandé pour confirmer la tolérance d’un corticoïde alternatif, quelle que soit la forme de la réaction.
Bibliographie
-
Angel-Pereira D, Berges-Gimeno MP, Madrigal-Burgaleta R, et al. Successful rapid desensitization to methylprednisolone sodium hemisuccinate. J Allergy Clin Immunol Pract. 2014;2(3):346-348.
-
Aranda A, Mayorga C, Ariza A, et al. IgE-mediated hypersensitivity reactions to methylprednisolone. Allergy. 2010;65(11):1376-1380.
-
Baeck M, Chemelle JA, Goossens A, Nicolas JF, Terreux R. Corticosteroid cross-reactivity: clinical and molecular modelling tools. Allergy. 2011;66(10):1367-1374.
-
Baeck M, Chemelle JA, Rasse C, Terreux R, Goossens A. C16-methyl corticosteroids are far less allergenic than the non-methylated molecules. Contact Dermatitis. 2011;64(6):305-312.
-
Baeck M, Chemelle JA, Terreux R, Drieghe J, Goossens A. Delayed hypersensitivity to corticosteroids in a series of 315 patients. Contact Dermatitis. 2009;61(3):163-175.
-
Baeck M, De Potter P, Goossens A. Allergic contact dermatitis following ocular use of corticosteroids. J Ocul Pharmacol Ther. 2011;27(1):83-92.
-
Baeck M, Goossens A. Patients with airborne sensitization/contact dermatitis from budesonide-containing aerosols « by proxy ». Contact Dermatitis. 2009;61(1):1-8.
-
Baeck M, Goossens A. Immediate and delayed allergic hypersensitivity to corticosteroids: practical guidelines. Contact Dermatitis. 2012;66(1):38-45.
-
Baeck M, Goossens A. Systemic contact dermatitis to corticosteroids. Allergy. 2012;67(12):1580-1585.
-
Baeck M, Marot L, Nicolas JF, Pilette C, Tennstedt D, Goossens A. Allergic hypersensitivity to topical and systemic corticosteroids: a review. Allergy. 2009;64(7):978-994.
-
Baeck M, Pilette C, Drieghe J, Goossens A. Allergic contact dermatitis to inhalation corticosteroids. Eur J Dermatol. 2010;20(1):102-108.
-
Baker A, Empson M, The R, Fitzharris P. Skin testing for immediate hypersensitivity to corticosteroids: a case series and literature review. Clin Exp Allergy. 2015;45(3):669-676.
-
Barbaud A. Place of excipients in systemic drug allergy. Immunol Allergy Clin North Am. 2014;34(3):671-679.
-
Barbaud A, Garvey LH, Torres M, et al. EAACI/ENDA position paper on drug provocation testing. Allergy. 2024;79(3):565-579.
-
Ben Said B, Leray V, Nicolas JF, Rozieres A, Berard F. Methylprednisolone-induced anaphylaxis: diagnosis by skin test and basophil activation test. Allergy. 2010;65(4):531-532.
-
Berbegal L, DeLeon FJ, Silvestre JF. Hypersensitivity reactions to corticosteroids. Actas Dermosifiliogr. 2016;107(2):107-115.
-
Bircher AJ, Thürlimann W, Hunziker T, et al. Contact hypersensitivity to corticosteroids in routine patch test patients. Dermatology. 1995;191(2):109-114.
-
Bjornsdottir HH, Einarsson OB, Gröndal G, Gudbjornsson B. Nationwide prevalence of glucocorticoid prescriptions over 17 years. SAGE Open Med. 2024;12:20503121241235056.
-
Boffa MJ, Wilkinson SM, Beck MH. Screening for corticosteroid contact hypersensitivity. Contact Dermatitis. 1995;33(3):149-151.
-
Borja JM, Galindo PA, Feo F, Gomez E. Urticaria to methylprednisolone sodium hemisuccinate. Allergy. 2001;56(8):791.
-
Bruusgaard-Mouritsen MA, Nasser S, Garvey LH, et al. Anaphylaxis to excipients in current clinical practice. Immunol Allergy Clin North Am. 2022;42(2):239-267.
-
Cadinha S, Malheiro D, Rodrigues J, et al. Delayed hypersensitivity reactions to corticosteroids. Allergol Immunopathol (Madr). 2005;33(6):329-332.
-
Coopman S, Degreef H, Dooms-Goossens A. Identification of cross-reaction patterns in allergic contact dermatitis from topical corticosteroids. Br J Dermatol. 1989;121(1):27-34.
-
Dooms-Goossens A, Andersen KE, Brandão FM, et al. Corticosteroid contact allergy: an EECDRG multicentre study. Contact Dermatitis. 1996;35(1):40-44.
-
Erdmann SM, Abuzahra F, Merk HF, et al. Anaphylaxis induced by glucocorticoids. J Am Board Fam Pract. 2005;18(2):143-146.
-
Freymond N, Catelain A, Queille E, et al. Allergic reaction to methylprednisolone. Rev Med Interne. 2003;24(10):698-700.
-
Gönül M, Gül U. Detection of contact hypersensitivity to corticosteroids in allergic contact dermatitis patients who do not respond to topical corticosteroids. Contact Dermatitis. 2005;53(2):67-70.
-
Hodgens A, Sharman T. Corticosteroids. In: StatPearls. StatPearls Publishing; 2025.
-
Isaksson M, Brandão FM, Bruze M, Goossens A. Recommendation to include budesonide and tixocortol pivalate in the European standard series. Contact Dermatitis. 2000;43(1):41-42.
-
Jacob SE, Steele T. Corticosteroid classes: a quick reference guide including patch test substances and cross-reactivity. J Am Acad Dermatol. 2006;54(4):723-727.
-
Kamel SI, Rosas HG, Gorbachova T. Local and systemic side effects of corticosteroid injections for musculoskeletal indications. AJR Am J Roentgenol. 2024;222(3):e2330458.
-
Klein-Gitelman MS, Pachman LM. Intravenous corticosteroids: adverse reactions are more variable than expected in children. J Rheumatol. 1998;25(10):1995-2002.
-
Kulberg A, Schliemann S, Elsner P. Contact dermatitis as a systemic disease. Clin Dermatol. 2014;32(3):414-419.
-
Li PH, Wagner A, Thomas I, et al. Steroid allergy: clinical features and the importance of excipient testing in a diagnostic algorithm. J Allergy Clin Immunol Pract. 2018;6(5):1655-1661.
-
Liu D, Ahmet A, Ward L, et al. A practical guide to the monitoring and management of the complications of systemic corticosteroid therapy. Allergy Asthma Clin Immunol. 2013;9(1):30.
-
Mahlab-Guri K, Asher I, Sthoeger Z. Immediate and delayed hypersensitivity reactions to corticosteroids — prevalence, diagnosis and treatment. Swiss Med Wkly. 2023;153:40025.
-
Matura M, Goossens A. Contact allergy to corticosteroids. Allergy. 2000;55(8):698-704.
-
Mendelson LM, Meltzer EO, Hamburger RN. Anaphylaxis-like reactions to corticosteroid therapy. J Allergy Clin Immunol. 1974;54(3):125-131.
-
Mur EC, Ballesteros MGC, Fernández RS, Marco CB. Generalized exanthematous reaction with pustulosis induced by topical corticosteroids. Contact Dermatitis. 2005;52(2):114-115.
-
Padial A, Posadas S, Alvarez J, et al. Nonimmediate reactions to systemic corticosteroids suggest an immunological mechanism. Allergy. 2005;60(5):665-670.
-
Patel A, Bahna SL. Immediate hypersensitivity reactions to corticosteroids. Ann Allergy Asthma Immunol. 2015;115(3):178-182.e3.
-
Pattrick M, Doherty M. Facial flushing after intra-articular injection of steroid. BMJ (Clin Res Ed). 1987;295(6610):1380.
-
Pecquet C. Pseudoallergie et flush aux corticoïdes. Rev Fr Allergol Immunol Clin. 2002;42(1):61-63.
-
Pirker C, Misić A, Frosch PJ. Angioedema and dysphagia caused by contact allergy to inhaled budesonide. Contact Dermatitis. 2003;49(2):77-79.
-
Pofi R, Caratti G, Ray DW, Tomlinson JW. Treating the side effects of exogenous glucocorticoids. Endocr Rev. 2023;44(6):975-1011.
-
Prescription Cost Analysis – England 2020-21. NHSBSA.
-
Stingeni L, Caraffini S, Assalve D, et al. Erythema-multiforme-like contact dermatitis from budesonide. Contact Dermatitis. 1996;34(2):154-155.
-
Svendsen SV, Bach RO, Mortz CG. Prevalence of contact allergy to corticosteroids in a Danish patient population. Contact Dermatitis. 2022;87(3):273-279.
-
Svendsen SV, Mortz CG. Contact allergy to corticosteroids: is the European baseline series sufficient? Contact Dermatitis. 2023;89(3):193-200.
-
Ventura MT, Calogiuri GF, Matino MG, et al. Alternative glucocorticoids for use in cases of adverse reaction to systemic glucocorticoids. Br J Dermatol. 2003;148(1):139-141.
-
Vijendra A, Shobnam N, Jordan J, et al. Biomarkers are consistent with patient-reported allergic sensitization in topical steroid withdrawal. Allergy. 2026;81(3):906-909.
-
Voltolini S, Fumagalli F. Delayed corticosteroid hypersensitivity: a clinical management proposal. Eur Ann Allergy Clin Immunol. 2021;53(4):171-176.
-
Walker AI, Räwer HC, Sieber W, Przybilla B. Immediate-type hypersensitivity to succinylated corticosteroids. Int Arch Allergy Immunol. 2010;155(1):86-92.
-
Wallace BI, Tsai H, Lin P, et al. Prevalence and prescribing patterns of oral corticosteroids in the United States, Taiwan, and Denmark, 2009–2018. Clin Transl Sci. 2023;16(12):2565-2576.
-
Wilkinson SM, Morrey K, Hollowood K, et al. HLA-A, -B and -DR antigens in hydrocortisone contact hypersensitivity. Contact Dermatitis. 1993;28(5):295-297.
Vous avez aimé cet article ?
Voici d'autres articles qui pourraient vous intéresser :